Suzuki K, Hayashi Y, Nakahara S, Kumazaki H, Prox J, Horiuchi K, Zheng M, Tanimura S, Nishiyama Y, Osawa S, Sehara-Fujisawa A, Saftig P, Yokoshima S, Fukuyama T, Matsuki N, Koyama R, Tomita T, Iwatsubo T: Activity-dependent proteolytic cleavage of neuroligin-1. Neuron 76:410-422, 2012
- 基礎
- 2012-10-18
- 264
新しい論文をNeuronに発表しました
Activity-Dependent Proteolytic Cleavage of Neuroligin-1
Kunimichi Suzuki, Yukari Hayashi, Soichiro Nakahara, Hiroshi Kumazaki, Johannes Prox, Keisuke Horiuchi, Mingshuo Zeng, Shun Tanimura, Yoshitake Nishiyama, Satoko Osawa, Atsuko Sehara-Fujisawa, Paul Saftig, Satoshi Yokoshima, Tohru Fukuyama, Norio Matsuki, Ryuta Koyama, Taisuke Tomita, Takeshi Iwatsubo
Neuron 76(2):410-422 (2012)
First Published on October 18, 2012, doi: 10.1016/j.neuron.2012.10.003
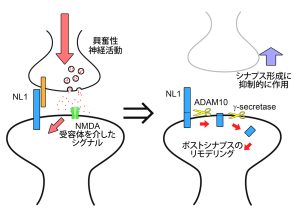
シナプスは神経活動に応じて結合様式や形を変えることが知られています。シナプス形成の異常は自閉症などの精神性疾患の原因となることが知られており、現在、シナプス形成に関わる分子の特定が盛んに行われています。しかし、いまだ不明の点が多く、特に、神経活動からシナプス形成までの一連の流れについてはほとんど調べられていませんでした。我々は、興奮性シナプス形成に必須の分子であり、自閉症の発症と関連が示されているシナプス膜タンパク質Neuroliginに着目しました。そして、まず興奮性の神経活動によって、タンパク質切断酵素であるプロテアーゼが活性化しNeuroliginが切断を受けること、その結果Neuroliginの量が減少して、神経細胞シナプス形成が制御されるという一連の流れを見出しました。また切断現象の責任プロテアーゼとしてADAM10とγセクレターゼの関与を明らかにしました。 本研究成果は、プロテアーゼによる、シナプス膜タンパク質切断がシナプスの形成と機能を制御している可能性を示した点で重要です。シナプス形成に関わる分子自体が、そもそもどのように制御を受けているのかを調べ、神経活動からシナプス形成までの全体像を初めて明らかにした成果です。今後、シナプス形成に関わる分子ではなく、その量を決めるプロテアーゼが、自閉症治療薬開発の重要な創薬標的分子となりうることも示唆されます。