Ito G, Fujimoto T, Kamikawaji S, Kuwahara T, Iwatsubo T: Lack of correlation between the kinase activity of LRRK2 harboring kinase-modifying mutations and its phosphorylation at Ser910, 935, and Ser955. PLoS One 9:e97988, 2014
- 基礎
- 2014-5-16
- 283
新しい論文をPLOS ONEに発表しました
Lack of correlation between the kinase activity of LRRK2 harboring kinase-modifying mutations and its phosphorylation at Ser910, 935, and Ser955
Genta Ito*, Tetta Fujimoto*, Shogo Kamikwaji*, Tomoki Kuwahara, Takeshi Iwatsubo (*equal contribution)
PLOS ONE 9(5),e97988 (2014) First Published on May 16, 2013, doi: 10.1371/journal.pone.0097988
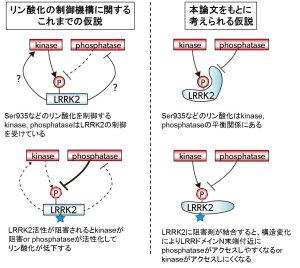
家族性パーキンソン病の責任遺伝子産物のひとつであるLeucine-rich repeat kinase 2(LRRK2)は細胞内の生理的条件下でリン酸化を受けます。LRRK2はキナーゼ活性を有し、細胞をLRRK2阻害剤で処理すると脱リン酸化されることから、LRRK2のリン酸化はLRRK2のキナーゼ活性により制御されていると考えられていました。本論文で、様々な変異体のリン酸化状態および阻害剤による脱リン酸化を解析したところ、キナーゼ活性をもたないT2035A変異体でも野生型LRRK2と同程度のリン酸化が生じ、野生型と同様にLRRK2阻害剤処理時に脱リン酸化されることを見出しました。この結果は、阻害剤処理による脱リン酸化がLRRK2下流シグナルの阻害によるという既存の仮説に反するものです。これらの知見をもとに、阻害剤処理による脱リン酸化の新たなメカニズムを追究することで、LRRK2リン酸化の生理的、病的役割の解明につながることが期待されます。