Matsumoto T, Matsukawa K, Watanabe N, Kishino Y, Kunugi H, Ihara R, Wakabayashi T, Hashimoto T, Iwatsubo T: Self-assembly of FUS through its low-complexity domain contributes to neurodegeneration. Hum Mol Genet 27: 1353-1365, 2018
- 基礎
- 2018-2-8
- 309
新しい論文をHuman Molecular Geneticsに発表しました
Self-assembly of FUS through its low-complexity domain contributes to neurodegeneration
Taisei Matsumoto*, Koji Matsukawa*, Naruaki Watanabe, Yuya Kishino, Hayato Kunugi, Ryoko Ihara, Tomoko Wakabayashi, Tadafumi Hashimoto, Takeshi Iwatsubo (*co-first author)
Human Molecular Genetics in press, first published on 7 February 2018, doi: 10.1093/hmg/ddy046
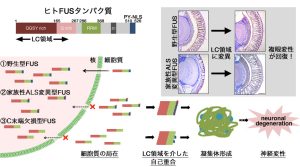
FUSは家族性筋萎縮性側索硬化症 (ALS)の病因遺伝子として、SOD1遺伝子に次いで頻度の高い遺伝子であり、またFUSタンパク質は、家族性及び孤発性ALSの運動ニューロンや、前頭側頭葉型変性症 (FTLD)患者の中枢神経細胞において、細胞内封入体として蓄積することが知られています。しかし、これまでFUSがどのようにALSやFTLDを発症させるか、その機序は未だ不明です。私たちはショウジョウバエの複眼に野生型あるいは家族性ALSを発現させることにより、進行性の神経細胞死を引き起こすモデル動物を作出し、まず、FUSの家族性ALS変異がFUSタンパク質を核内から細胞質へ移行させると共に、神経細胞死を増悪させることを見出しました。さらに、FUSのアミノ末端に存在する、アミノ酸残基の種類が乏しいlow-complexity (LC)領域に注目し、LC領域の27個のチロシン残基を全てセリン残基に変異させたallS変異は、FUS同士の自己重合能を喪失させ、さらに神経細胞死を抑制することを明らかにしました。この結果は、FUSが細胞質においてLC領域を介して自己重合することにより、神経毒性を発揮する可能性を示唆しており、今後ALSやFTLDの病因解明、さらに、重篤な神経難病であるALSの根本治療薬開発に重要な知見を与えるものであります。 論文へのリンクはこちら