Eguchi T, Sakurai M, Wang Y, Saito C, Yoshii G, Wileman T, Mizushima N, Kuwahara T, Iwatsubo T: The V-ATPase-ATG16L1 axis recruits LRRK2 to facilitate lysosomal stress responses. J Cell Biol 223(3):e202302067, 2024
- 基礎
- 2024-1-17
- 372
新しい論文をJournal of Cell Biologyに発表しました
The V-ATPase-ATG16L1 axis recruits LRRK2 to facilitate the lysosomal stress response
Tomoya Eguchi*, Maria Sakurai*, Yingxue Wang, Chieko Saito, Gen Yoshii, Thomas Wileman, Noboru Mizushima, Tomoki Kuwahara, Takeshi Iwatsubo (*co-first author)
J. Cell Biol. 223(3):e202302067, 2024, doi: 10.1083/jcb.202302067
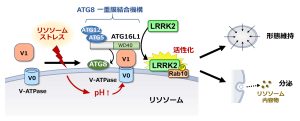
LRRK2は家族性および孤発性パーキンソン病(PD)にかかわるタンパク質リン酸化酵素(キナーゼ)であり、その異常な活性化がPDの背景にあることが示唆されています。LRRK2はストレスを受けたリソソーム上に局在化することで活性化しますが、そのメカニズムは多くが不明でした。今回私たちは、オートファジーに必須の機構として従来知られていた「ATG8結合系」が、オートファジーとは異なる「ATG8 一重膜結合機構」を介して、LRRK2をリソソーム上に局在化させることを見出しました。特に、この機構の詳細な分子メカニズムとして近年報告された「V-ATPase-ATG16L1軸」が、LRRK2のリソソーム膜局在化および活性化を制御することが分かりました。さらにこの機構は、LRRK2活性化を介してリソソームストレス応答に働き、ストレスを受けたリソソームの形態調節や内容物放出をもたらすことが分かりました。これらの結果は、LRRK2の異常活性化機構の理解につながるとともに、そのメカニズムへの介在がPDの治療戦略になる可能性を示すものです。本研究は東大・水島研究室および英国East Anglia大学との共同研究として行われました。 論文へのリンクはこちら。 プレスリリースはこちら。 日本経済新聞、文教速報デジタル版 解説記事をAutophagy誌に発表しました。(2024.3.19)