Eguchi T, Kuwahara T, Sakurai M, Komori T, Fujimoto T, Ito G, Yoshimura SI, Harada A, Fukuda M, Koike M, Iwatsubo T: LRRK2 and its substrate Rab GTPases are sequentially targeted onto stressed lysosomes and maintain their homeostasis. Proc Natl Acad Sci USA 115:E9115-E9124, 2018
- 基礎
- 2018-9-13
- 312
新しい論文をProceedings of the National Academy of Sciences of the United States of America (PNAS) に発表しました
パーキンソン病 病因タンパク質LRRK2の関わる新規ストレス応答機構の発見 LRRK2 and its substrate Rab GTPases are sequentially targeted onto stressed lysosomes and maintain their homeostasis
Tomoya Eguchi*, Tomoki Kuwahara*, Maria Sakurai*, Tadayuki Komori, Tetta Fujimoto, Genta Ito, Shin-ichiro Yoshimura, Akihiro Harada, Mitsunori Fukuda, Masato Koike, and Takeshi Iwatsubo (*co-first author)
PNAS published ahead of print September 12, 2018, https://doi.org/10.1073/pnas.1812196115 (open access)
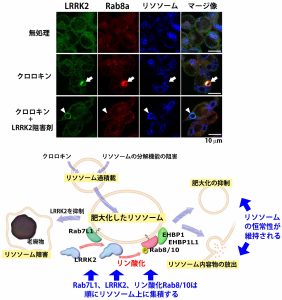
LRRK2(leucine-rich repeat kinase 2)は家族性パーキンソン病の病因遺伝子産物であり、その機能を明らかにすることがパーキンソン病治療法開発の鍵になると考えられます。LRRK2はキナーゼ活性を有し、近年、当研究室を含めた複数のグループから、細胞内における基質として一部のRabファミリー低分子量Gタンパク質(Rab8a, Rab10, Rab7L1など)が報告されました。しかしLRRK2によるRabリン酸化の役割については不明でした。一方、Lrrk2の欠損マウスでは腎臓や肺において肥大したリソソームの蓄積を認めることから、LRRK2とリソソームとの関連が示唆されてきました。今回、私達はLRRK2と基質Rabがリソソームに対するストレスに応答してリソソーム膜上に集積し、リソソームの恒常性を維持することを発見しました。その機構として、リソソームが過積載状態になり肥大化すると、まずRab7L1とLRRK2が順にリソソーム膜上に局在化し、LRRK2のキナーゼ活性が亢進すること、次にRab8aとRab10がLRRK2によるリン酸化を受けてリソソーム膜上に集積し、相互作用因子であるEHBP1とEHBP1L1を動員してリソソームの肥大化抑制とリソソーム内容物の細胞外放出を引き起こすことを明らかにしました。この発見は、リソソームがストレスに応答する新たな機構を提唱するものであると同時に、病因タンパク質の分解障害や細胞外への放出などの、パーキンソン病の病態メカニズムの理解と治療法の開発にもつながるものと期待されます。本研究は、順天堂大学・小池正人教授、東北大学・福田光則教授、大阪大学・原田彰宏教授との共同研究の成果です。 論文へのリンクはこちら。 東京大学からのプレスリリースはこちら。 本研究成果はAlzforum、日経バイオテク、日本経済新聞、日刊工業新聞に掲載されました。