Kamikawaji S, Ito G, Sano T, Iwatsubo T: Differential effects of familial parkinson mutations in LRRK2 revealed by a systematic analysis of autophosphorylation. Biochemistry 52:6052-6062, 2013
- 基礎
- 2013-8-8
- 275
新しい論文をBiochemistryに発表しました
Shogo Kamikawaji*, Genta Ito*, Tomoko Sano, and Takeshi Iwatsubo(*equal contribution)
Biochemistry 52(35): 6052-6062, 2013
First Published on August 8, 2013, doi: 10.1021/bi400596m
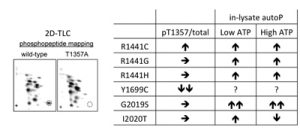
Leucine-rich repeat kinase 2(LRRK2)は家族性パーキンソン病(FPD; PARK8)の病因遺伝子産物です。現在までに、R1441C/G/H、Y1699C、G2019S、I2020Tの6種類のアミノ酸置換がPARK8の原因となることが知られていますが、そのメカニズムはよくわかっていません。今回私たちは、2次元薄層クロマトグラフィーによるホスホペプチドマッピングを行い、LRRK2の主要な自己リン酸化部位としてThr1348、Thr1349、Thr1357を同定しました。また、Y1699C変異によりThr1357における自己リン酸化が選択的に抑制されること、低濃度のATP存在下において、解析対象外のY1699C変異体を除くすべての変異体が野生型に比して高い自己リン酸化能を発揮することを発見しました。これらの結果から、細胞内ATP濃度が異常に低下した条件下では、FPD変異型LRRK2は野生型LRRK2より高いキナーゼ活性を発揮する可能性が示唆されました。そのような条件下で過剰リン酸化される基質タンパク質の探索から、FPD変異型LRRK2が神経変性を引き起こす分子メカニズムの解明につながる重要な知見です。