Morohashi Y, Kan T, Tominari Y, Fuwa H, Okamura Y, Watanabe N, Sato C, Natsugari H, Fukuyama T, Iwatsubo T, Tomita T: Carboxyl-terminal fragment of presenilin is the molecular target of a dipeptidic γ-secretase-specific inhibitor DAPT. J Biol Chem 281: 14670-14676, 2006
- 基礎
- 2006-3-28
- 184
新しい論文をThe Journal of Biological Chemistryに発表しました
Yuichi Morohashi, Toshiyuki Kan, Yusuke Tominari, Haruhiko Fuwa, Yumiko Okamura, Naoto Watanabe, Chihiro Sato, Hideaki Natsugari, Tohru Fukuyama, Takeshi Iwatsubo, Taisuke Tomita
The Journal of Biological Chemistry 281(21):14670-14676 (2006)
First Published on March 28, 2006, doi: 10.1074/jbc.M513012200
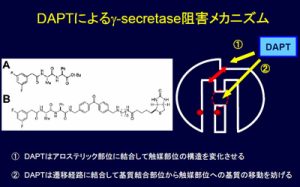
γセクレターゼ阻害剤がどのような分子メカニズムによって酵素活性を阻害するかということは、新規阻害剤の探索のみならず、その切断機構の理解の上で重要です。今回γ-secretase特異的阻害剤であるDAPT(A)に、光親和性標識基・ビオチン基を導入したDAP-BpB(B)の合成に成功しました。そしてこの化合物を分子プローブとして用い、DAPTの標的分子がプレセニリンC末端断片であり、基質が活性中心に移行する過程を阻害している可能性を見出しました。本研究はこれまで作用点が明らかでなかったDAPTの作用機序を世界で初めて明らかにしたと同時に、ケミカルバイオロジー的アプローチによってγ-secretaseの切断機構の一端を明らかにしたという意味で、有意義な研究成果です。今後同様の手法により、様々な化合物の作用機序を明らかにすることができるものと期待されます。本研究は、本学COEプロジェクトの一つとして行われた、天然物合成化学教室・創薬理論科学教室との共同研究成果です。