Watanabe N, Takagi S, Tomita T, Iwatsubo T: Functional analysis of the transmembrane domains of presenilin 1: participation of transmembrane domains 2 and 6 in the formation of initial substrate binding site of γ-secretase. J Biol Chem 285:19738-19746, 2010
- 基礎
- 2010-4-23
- 244
新しい論文をThe Journal of Biological Chemistryに発表しました
Naoto Watanabe, Shizuka Takagi, Aya Tominaga, Taisuke Tomita, Takeshi Iwatsubo
The Journal of Biological Chemistry 285(26):19738-19746 (2010)
First Published on April 23, 2010, doi: 10.1074/jbc.M110.101287
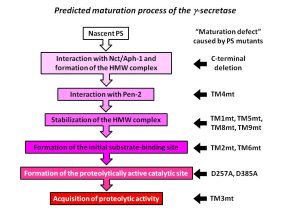
γセクレターゼはプレセニリン、ニカストリン、Aph-1、Pen-2を最小構成因子とする膜蛋白複合体です。活性中心サブユニットであるプレセニリンには活性中心ポア構造の他、基質を脂質二重膜内で側方より捕捉する基質結合部位(Initial substrate-binding site)の存在が示唆されています。本研究においてはシステマチックにプレセニリン1(PS1)の膜貫通領域(TMD)を置換してその変異体の機能解析を行う、以前の研究(Watanabe et al., JBC 2005)をさらに進めました。そして各TMDが活性型γセクレターゼ形成過程において果たす役割について明らかにしました(スキーム)。また化合物を利用したケミカルバイオロジーや、システインを用いたクロスリンク実験などを活用し、TMD2とTMD6がPS1の基質結合部位形成に重要であることを明らかにしました。PSの基質結合部位の詳細を明らかにすることによって、基質特異的なγセクレターゼ活性制御、すなわち、副作用の少ないアルツハイマー病治療薬創成につながる可能性があります。